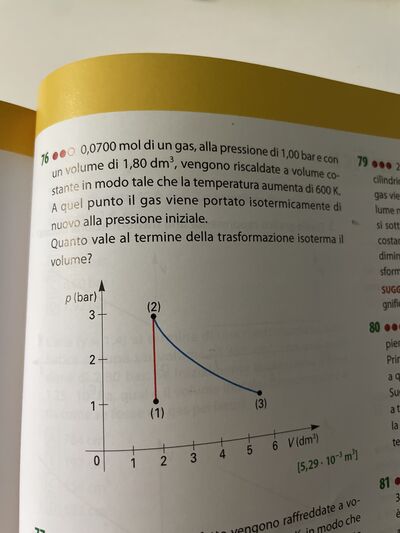
$0,0700 \mathrm{~mol}$ di un gas, alla pressione di 1,00 bar econ un volume di $1,80 \mathrm{dm}^3$, vengono riscaldate a volume costante in modo tale che la temperatura aumenta di $600 \mathrm{~K}$. A quel punto il gas viene portato isotermicamente di nuovo alla pressione iniziale.
Quanto vale al termine della trasformazione isoterma il volume?