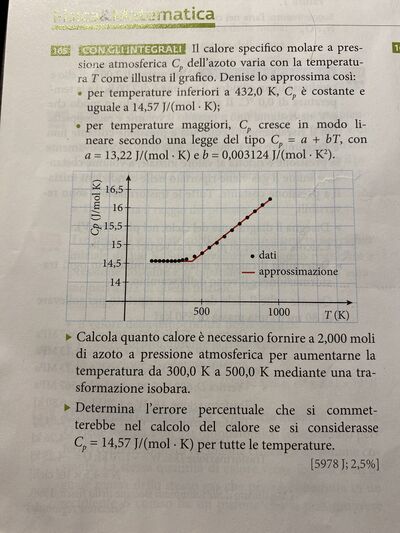
Il calore specifico molare a pres- sione atmosferica $C_p$ dell'azoto varia con la temperatura $T$ come illustra il grafico. Denise lo approssima così:
- per temperature inferiori a $432,0 \mathrm{~K}, C_p$ è costante e uguale a $14,57 \mathrm{~J} /(\mathrm{mol} \cdot \mathrm{K})$;
- per temperature maggiori, $C_p$ cresce in modo lineare secondo una legge del tipo $C_p=a+b T$, con $a=13,22 \mathrm{~J} /(\mathrm{mol} \cdot \mathrm{K})$ e $b=0,003124 \mathrm{~J} /\left(\mathrm{mol} \cdot \mathrm{K}^2\right)$.
Calcola quanto calore è necessario fornire a 2,000 moli di azoto a pressione atmosferica per aumentarne la temperatura da $300,0 \mathrm{~K}$ a $500,0 \mathrm{~K}$ mediante una trasformazione isobara.
Determina l'errore percentuale che si commetterebbe nel calcolo del calore se si considerasse $C_p=14,57 \mathrm{~J} /(\mathrm{mol} \cdot \mathrm{K})$ per tutte le temperature.
$[5978] ; 2,5 \%]$
Trasformazioni termodinamiche