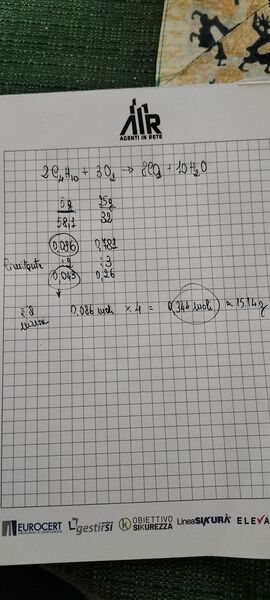Calcola la quantità di $\mathrm{CO}_2$ che si ottiene nella reazione tra $5,0 \mathrm{~g}$ di butano $\mathrm{C}_4 \mathrm{H}_{10}$ e $25,0 \mathrm{~g}$ di $\mathrm{O}_2$.
$$
2 \mathrm{C}_4 \mathrm{H}_{10(\mathrm{~g})}+3 \mathrm{O}_{2(\mathrm{~g})} \longrightarrow 8 \mathrm{CO}_{2(\mathrm{~g})}+10 \mathrm{H}_2 \mathrm{O}_{(\mathrm{g})}
$$