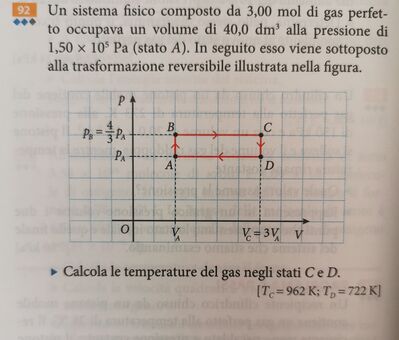
Trova TA con la legge dei gas perfetti.
Pa * VA = n R TA;
R = 8,314 J/molK.
La pressione è data in Pascal, il volume in dm^3, non va bene.
Il volume deve essere in m^3 se la pressione è in Pascal.
40,0 dm^3 = 40,0 * 10^-3 m^3;
TA = PA * VA / (n R);
TA = 1,50 * 10^5 * 40,0 * 10^-3 / (3,00 * 8,314) = 241 K;
Da A a B la trasformazione è isovolumica, VA = VB = costante.
La pressione aumenta di 4/3, aumenta proporzionalmente anche la temperatura, aumenta anch'essa di 4/3.
Scriviamo la proporzione:
TB : PB = TA : PA;
TB : (4/3 PA) = 241 : PA;
TB = 4/3 PA * 241 / PA;
TB = 4/3 * 241 = 321 K;
Da B a C la trasformazione è isobara, PB = PC = costante.
Il volume aumenta di 3 volte; VC = 3VB = 3 VA, anche la temperatura aumenta di 3 volte.
TC : VC = TB : VB;
TC : 3 VA = 321 : VA;
TC = 3 VA * 321 / VA = 3 * 321 = 963 K (circa).
Da C a D, il volume è costante, variano pressione e temperatura;
la pressione diminuisce di 4/3 quindi anche la temperatura diminuisce di 4/3. PD = PA
TD : PD = TC : PC;
TD : PA = 963 : (4/3 PA);
TD = PA * 963 : (4/3 PA);
TD = 963 * 3/4 = 722 K.
Ciao @angela_chen
Devi studiare le trasformazioni termodinamiche: isobara, isovolumica; isoterma....
https://argomentidifisica.wordpress.com/2010/03/17/i-principi-della-termodinamica/