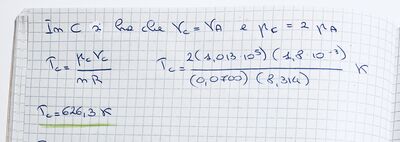buonasera qualcuno sa risolvere questo problema disegnando il grafico grazie in anticipo
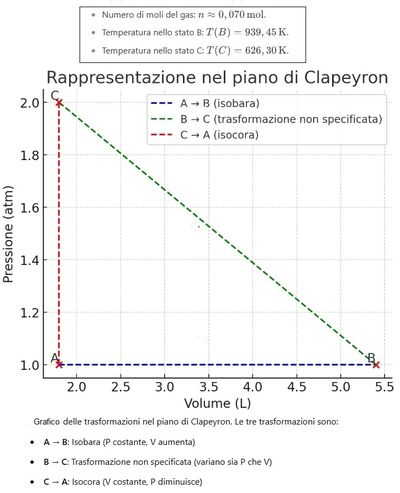
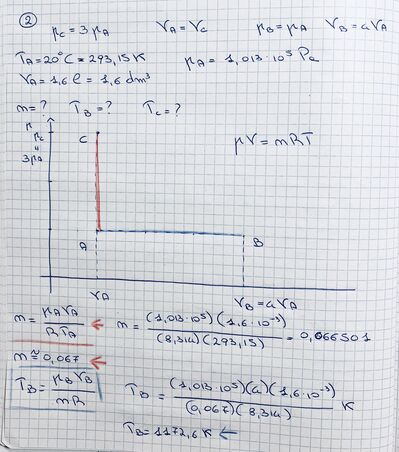
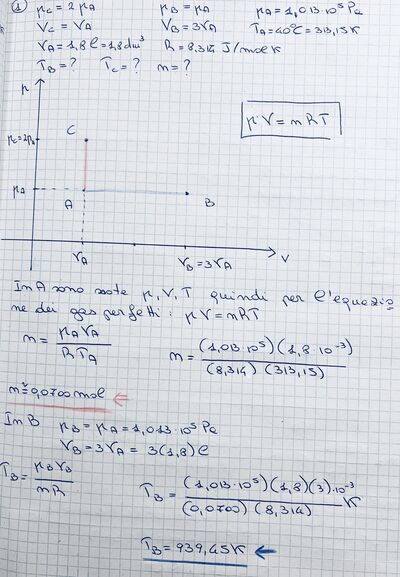
Nel piano di Clapeyron si hanno degli stati termodinamici tali che: PC - 2PA, VA - VC, PB - PA, VB - 3VA. Sapendo che in A la pressione è quella atmosferica e la temperatura 40 °C, determina la temperatura negli stati B,C.
Se nello stato A il volume del gas è di 1,80 L, quante sono le moli del gas? (R = 8,314 J/mol K)