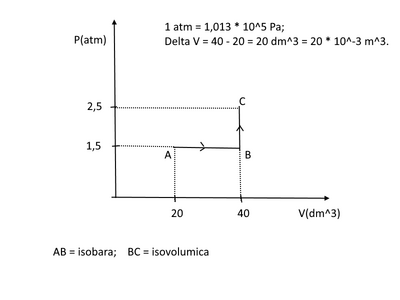
Una mole di un gas perfetto che si trova nello stato $A$ (pressione $=1,5 \mathrm{~atm}$; volume $=20 \mathrm{dm}^3$ ) effettua una doppia trasformazione: a pressione costante passa allo stato $B$ (volume $=40 \mathrm{dm}^3$ ), poi a volume costante passa allo stato $C$ (pressione $=2,5 \mathrm{~atm}$ ).
Durante la trasformazione $A B C$, l'energia interna del gas aumenta di $10600 \mathrm{~J}$.
- Rappresenta la trasformazione nel piano $p-V$.
- Qual è il lavoro totale durante la trasformazione $A B C$ ?
- Quanto vale il calore scambiato?
[3,0 kJ; 13,6 kJ]
Es 41