P V = n R T
TA = PV / (n R);
Se V è dato in litri e la pressione P è in atmosfere la costante R ha valore:
R = 0,0821 litri atm/molK;
n = 1 mole;
TA = 1 * 2 / (1 * 0,0821) = 24,4 K;
ΔUU = 1200 J;
ΔU = cv n (TD - TA);
ΔU = variazione di energia interna, è data in Joule, qui R deve essere 8,314 J/molK;
ΔU dipende dalla variazione di temperatura
cv = 3/2 R, calore specifico a volume costante; R deve essere 8,314 J/molK;
cv = 1,5 * 8,314 = 12,471 J /molK
TD - TA = ΔU / (cv n) = 1200 / 12,471 = 96 K;
TD = 96,2 + TA = 96 + 24,4 = 120,4 K; circa 120 K.
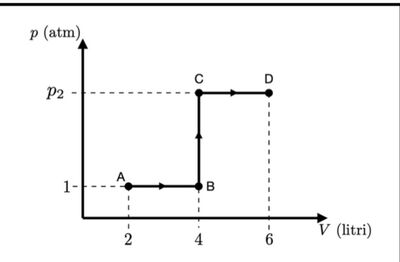
Pressione nello stato D; VD = 6 litri;
P2 = n R TD / VD = 1 * 0,0821 * 120 / 6 = 1,64 atm;
Lavoro da A a B, isobara; se vogliamo il lavoro in Joule, il volume deve essere in m^3 e la pressione in Pascal;
P1 = 1 atm= 1,013 * 10^5 Pa;
ΔV = (4 - 2) litri = 2 * 10^-3 m^3;
LAB = P1 * ΔV = 1,013 * 10^5 * 2 * 10^-3 = 203 J;
Da B a C, isovolumica, il lavoro è nullo;
Da C a D, di nuovo isobara:
L CD = P2 * ΔV = (1,64 * 1,013 * 10^5 Pa) * (6 - 4) * 10^-3 m^3;
L CD = 332 J;
L = 203 + 332 = 535 J (circa).
Ciao @gaiapp