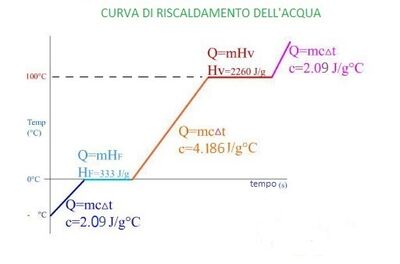
Q = c * m * (T equilibrio - T iniziale); calore.
calore specifico del ghiaccio e dell'acqua:
c1= 4186 J/kg°C, (acqua m1 a 25°C); cede calore;
m1 = 1 kg di acqua; (1 litro = 1 dm^3 = 1 kg).
c2 = 2090 J/kg°C; ghiaccio da - 60°C fino a 0°C;poi fonde; assorbe calore;
calore latente di fusione λf = 3,34 * 10^5 J/kg;
m2 = 0,050 kg;
Q fusione = λf * m2 = + 3,34 * 10^5 * 0,050 = 16700 J; calore assorbito;
m2 (il ghiaccio), diventa acqua fredda a 0°C ; assorbe calore, si scalda fino a temperatura di equilibrio, Te.
Q3 = c1 * m2 * (Te - 0°);
Q1 + Q2 + Q fusione + Q3
c1*m1*(Te - 25°) + c2 * m2 * [0°-(- 60°)] + λf * m2 + c1* m2*(Te - 0°) = 0;
4186 *1* (Te - 25°) + 2090 * 0,050 * 60° + 16700 + 4186 * 0,050 * Te = 0;
4186 Te - 104650 + 6270 + 16700 + 209,3 Te = 0;
4186 Te + 209,3 Te = + 104650 - 6270 - 16700;
4395,3 Te = 81680;
Te = 81680 / 4395,3 = 18,6°C, (Temperatura finale di equilibrio).
Massa d'acqua = 1 kg + 0,050 kg = 1,050 kg
Massa d'acqua = 1050 grammi.
@green ciao